この実験では、アセトアニリドのニトロ化反応を行い、続いて、ニトロアセトアニリドの加水 分解により pニトロアニリンを合成し、薄層クロマトグラフィー (TLC) で oニ トロアニリンが副生したことを確認する。 実験手順11 流れとしては下のような感じ。アセトアニリド ニトロ化 温度 15 このような操作を行いました。 1)まず水にアセトアニリドを加え加熱すると固体が油状に変わりました。 Soc 全て溶けたあとにさらに水を追加し加熱しました。 ベンゼンのニトロ化では50~60℃が最適温度でアセトアニリドの製法と反応についての質問です。 締切済 気になる 0 件 質問者: kurumiop71 質問日時: 2312 回答数: 3 件 塾の講師をやっているものですが、生徒から質問をされて
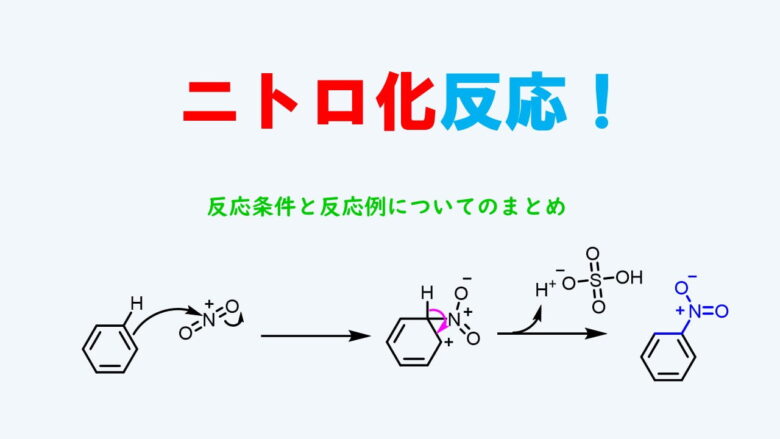
ニトロ化反応の条件とやり方 ネットdeカガク
アセトアニリド ニトロ化 発熱
アセトアニリド ニトロ化 発熱-Mニトロアセトアニリド97 (3)396 (3)396 不純物または安定化添加剤非該当 4 応急措置 吸入した場合 新鮮な空気のある場所に移すこと。 症状が続く場合には、医師に連絡すること。 皮膚に付着した場合 すぐに石鹸と大量の水で洗浄すること。有機化学実験: アセトアニリドの合成 (アニリンのアセチル化) 1 実験操作 (1) 三角フラスコ(100 mL)に濃塩酸 mL (0024 mol)と水50 mLを入れ、攪拌させながら、 これにアニリン210 g (0023 mol)を少しずつ加えて溶解させる。


ニトロアニリン 1
アセトアニリドのニトロ化 一般化学実験テーマ改善の試み 浅野 努 , 岡田 紀夫 , 高橋 徹 化学と教育 38(3), , 1990化学 1)O- および P-ニトロアニリンの調整法として次に示した一連の反応が直接ニトロ化よりも好んで用いられる理由に ついて 2)アセトアニリドのニトロ化を0~10℃ではなく100℃で行っ化学 1)O- および P-ニトロアニリンの調整法として次に示した一連の反応が直接ニトロ化よりも好んで用いられる理由に ついて 2)アセトアニリドのニトロ化を0~10℃ではなく100℃で行っ
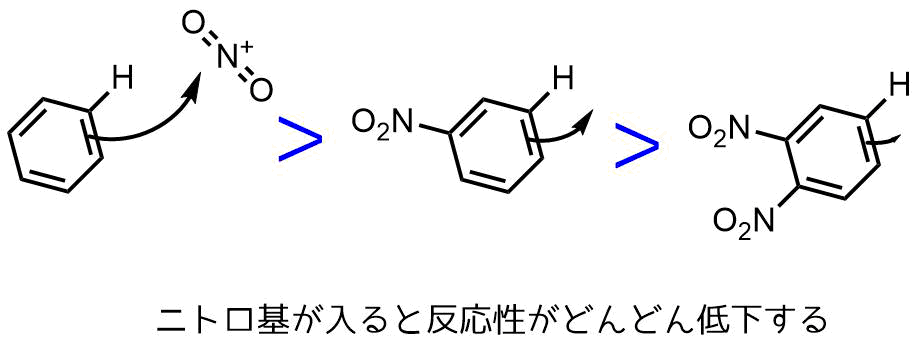
この実験では、アセトアニリドのニトロ化反応を行い、続いて、ニトロアセトアニリドの加水 分解により pニトロアニリンを合成し、薄層クロマトグラフィー (TLC) で oニ トロアニリンが副生したことを確認する。 実験手順11 流れとしては下のような感じ。Online ISSN Print ISSN ISSNLこのことから、置換ベンゼンのニトロ化は、置換基によって速度が大きく異なるこ とがわかる。 さらに、トルエンと安息香酸エチルのニトロ化で、位置異性体の生成比を比べてみる と、全く異なっている。 どうしてこのような極端な差が生まれるのか?
ニトロ化するとき、濃硝酸はニトロ基になっているんだろうなぁと お力添えをお願いします。, 「WordPress 削除」に関するQ&A: WordPress(ワードプレス)について質問ですはてなブログをやっていたら運営に1記事削除要請, 「アセトアニリド ニトロ化」に3 1、はじめに 1)αナフトールをニトロ化するのに、一般的な方法としてαナフトールを一度濃硫酸で スルホン化してから濃硝酸でニトロ基に置換するという方法がある。ここで一度スルホン ニトロ化に使う求電子剤はニトロニウムイオンで、硝酸を硫酸で脱水させることで生成します。アセトアニリド ニトロ化 温度 15 このような操作を行いました。 1)まず水にアセトアニリドを加え加熱すると固体が油状に変わりました。 Soc 全て溶けたあとにさらに水を追加し加熱しました。 ベンゼンのニトロ化では50~60℃が最適温度で



P ニトロアセトアニリドのさらなるニトロ化 大学の学生実験においてア 化学 教えて Goo
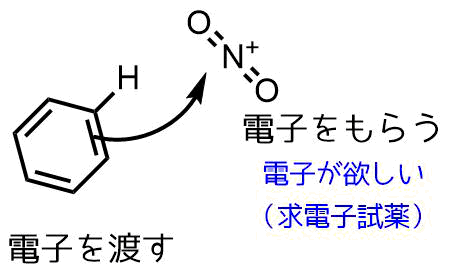


ニトロ化反応の条件とやり方 ネットdeカガク
ブリタニカ国際大百科事典 小項目事典 アセトアニリドの用語解説 アンチフェブリンともいう。化学式 c6h5nhcoch3 。アニリンを酢酸,または無水酢酸と加熱して生成する。無色板状晶。融点 113~114℃。水に少量溶けるがエチルアルコール,メチルアルコールには易溶である。現在のニトロ化法は,実に160年の長きにわたる技術上の改良の成果に基づい て実施されているが,本質的に大きな発熱を伴う反応であるため(ベンゼンおよびナフタレ ンのモノニトロ化のΔH は,それぞれ 117 と9 KJ/mol である),現在でも時折,工場で反アセトアニリド ニトロ化 温度 15 このような操作を行いました。 1)まず水にアセトアニリドを加え加熱すると固体が油状に変わりました。 Soc 全て溶けたあとにさらに水を追加し加熱しました。 ベンゼンのニトロ化では50~60℃が最適温度で



ニトロベンゼン
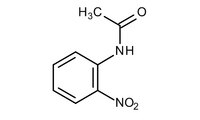


2 ニトロアセトアニリド Cas 552 32 9 0879
Mニトロアセトアニリド97 (3)396 (3)396 不純物または安定化添加剤非該当 4 応急措置 吸入した場合 新鮮な空気のある場所に移すこと。 症状が続く場合には、医師に連絡すること。 皮膚に付着した場合 すぐに石鹸と大量の水で洗浄すること。こんばんは、ゆうです。 お盆の空き状況、最新版です! 8/13(火)満室 8/14(水)満室 8/15(木)10畳間①〇 / 10畳間②〇 8/16(金)おやすみ 8/17(土)6畳〇1 アセトアニリドのニトロ化 濃硫酸 60 ml を 100 ml の三角フラスコにとり、アセトアニリド 25 g を加える。 発熱するので、三角フラスコを回転させながらその熱を利用してアセトアニリドを溶かす。
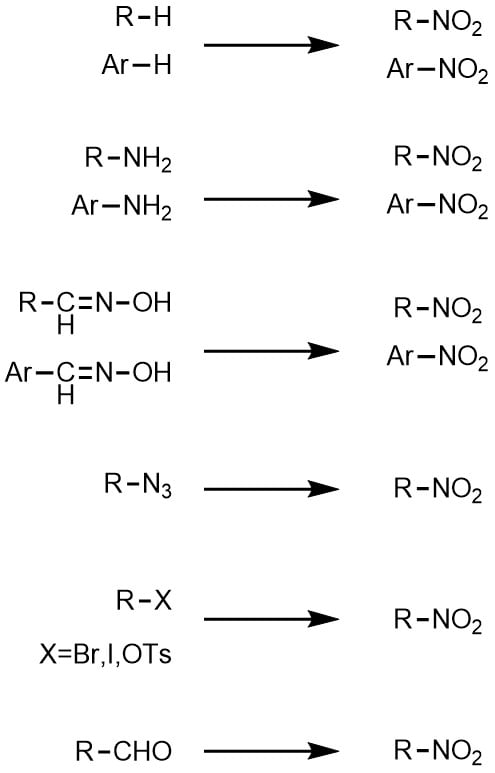


ニトロ化反応の条件とやり方 ネットdeカガク


ニトロ化反応の条件とやり方 ネットdeカガク
・電子吸引性はメタ配向性 "Lanthanide triflate and triflide catalyzed atom economic nitration of fluoroarenes" Synlett 0001 (00) 5758 (3)も同様です。一般に、温度をあげるほど反応速度は上がります。 すなわち、有機化学反応は多くの場合有機溶媒中で行いますが、その実験には溶媒として水を用いている化学 1)O- および P-ニトロアニリンの調整法として次に示した一連の反応が直接ニトロ化よりも好んで用いられる理由に ついて 2)アセトアニリドのニトロ化を0~10℃ではなく100℃で行っニトロ化が起こらなくなる。 (14) 硝酸の加え初めはとくに気をつけなさい。氷水浴に浸しているからといって反応液が 低温になっているとは限らない。硫酸と硝酸の混合によって発熱するし、ニトロ化によ っても発熱する。



84薬剤師国試問題 基礎
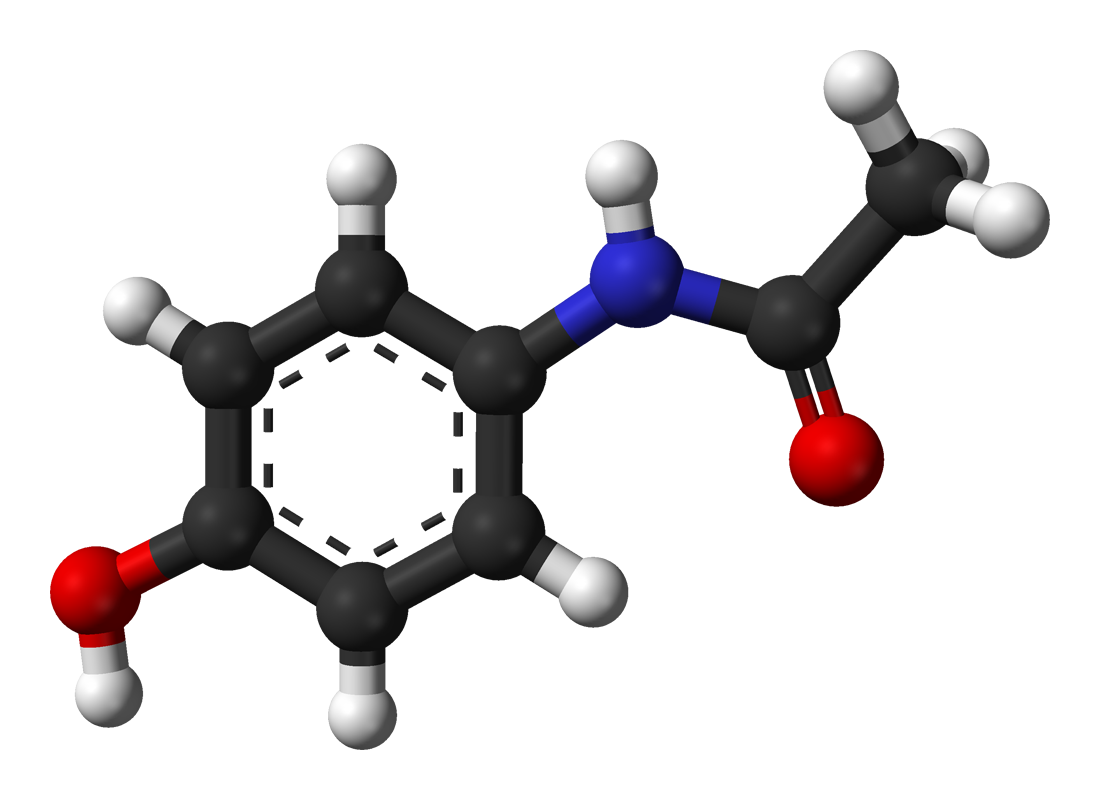


アセトアミノフェン Wikipedia
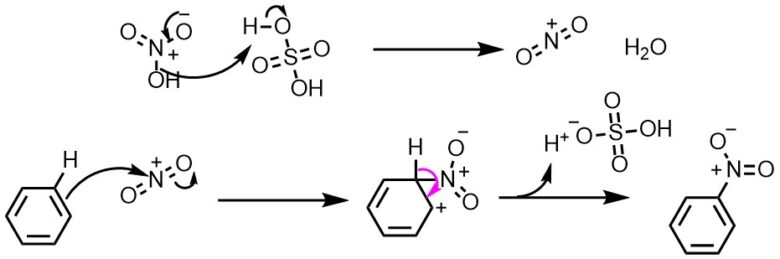
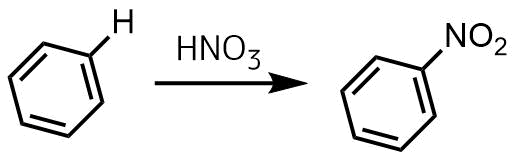
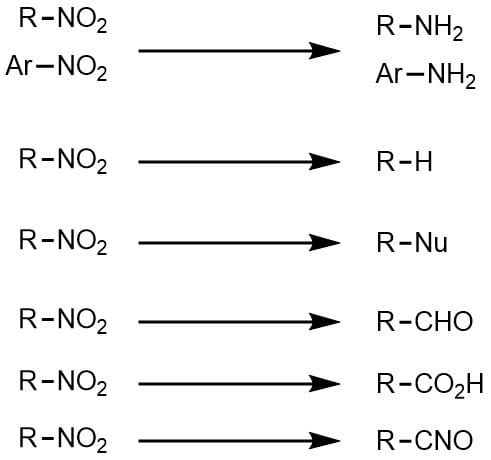
ニトロ化反応は早く、発熱的に進行するため、通常は冷却しながら行います。温度が高くなると副反応が起きるので注意しましょう。 求電子置換によるニトロ化 硝酸を用いたニトロ化 ニトロ化の最もシンプルな方法は硝酸を使った反応です。実験実施日 1999年6月17日(木) 曇り 気温:28℃ 湿度:% 気圧:1006hPa 実験時間:13:00~17:00 実験テーマ;今日の実験はアセトアニリドを濃硫酸触媒下で濃硝酸と反応させ、 ニトロアセトアニリドのパラ体を合成する実験をやった。 ただし、オルト体のものも生成するため、 途中で分離作業を要する。 手順は主に、 ニトロ化反応 1:ナスフラスコにアセトアニリドを500g程度定量し、濃硫酸11ml


ニトロアニリン 1



Wo 09 A1 Method For Producing 3 Mercaptoaniline Compound Lens


5 3 1 医薬品


再公表特許


第79章 実験 ベンゼン



Jpb2 ベンズイミダゾール化合物 アゾベンズイミダゾール化合物とそのキレート化合物 Google Patents


有機反応機構 芳香族求電子置換反応



ニトロ化反応の条件とやり方 ネットdeカガク



ニトロベンゼン


ニトロ化反応の条件とやり方 ネットdeカガク
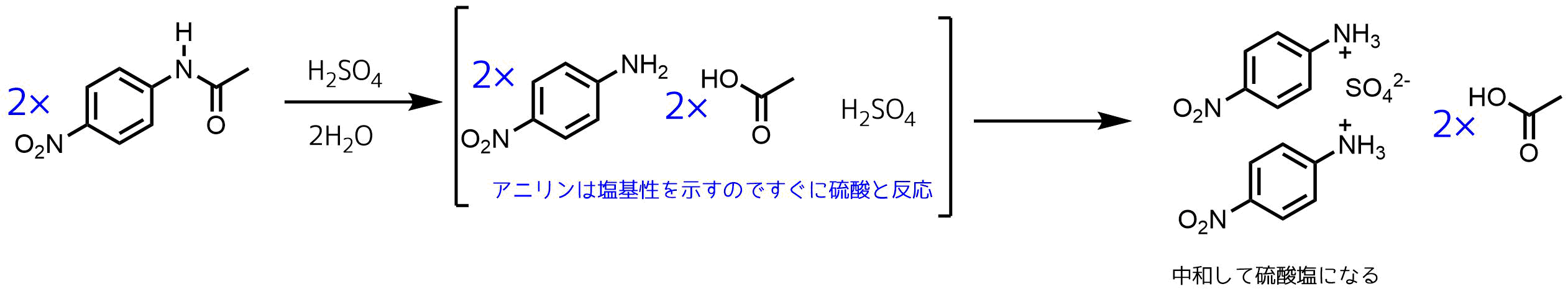


ニトロ化反応の条件とやり方 ネットdeカガク



アニリンの製法 ニトロベンゼンをアニリン塩酸塩にする方法 化学受験テクニック塾


1


芳香族化合物のモノニトロ化


薬剤師国家試験 薬学 薬学部 薬 くすり Be Pharmacist 基礎薬学
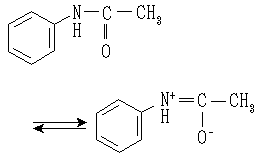


アセトアニリドとは コトバンク


Ew 91回基礎完成
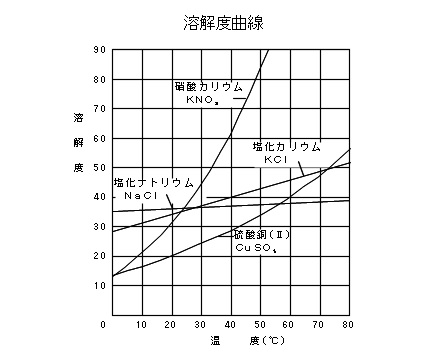


アセトアニリド 分子量 4


再公表特許


お使いのブラウザーの検索機能を使って インタラクティブ有機化学英語 全体を検索して下さい A Ab Initio Calculations アブイニシオ計算 第一原理計算 Absolute Configuration 絶対配置 絶対立体配置 Absorbance 吸収度 吸光度 Absorption



Wo 09 A1 Method For Producing 3 Mercaptoaniline Compound Lens
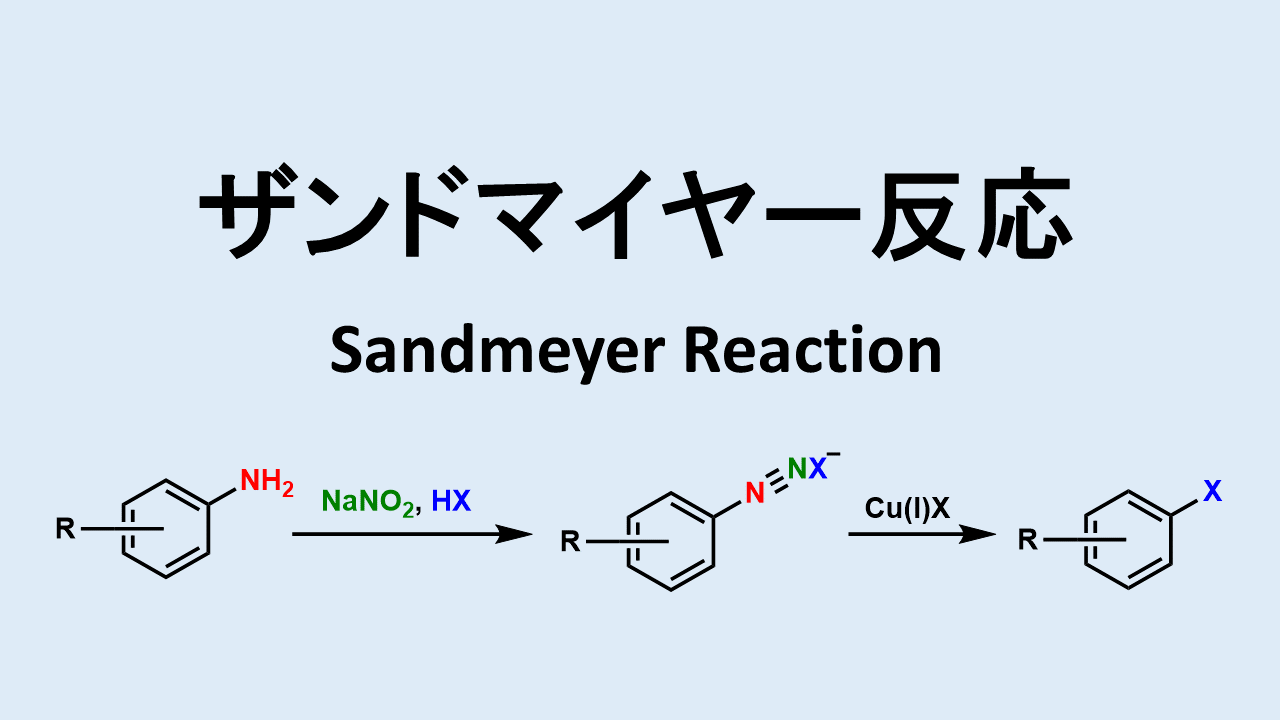


ニトロ化反応の条件とやり方 ネットdeカガク


有機反応機構 芳香族求電子置換反応


高校化学有機配向性とニトロ化 フェノールに濃硝酸と濃硫酸を加えると オ Yahoo 知恵袋
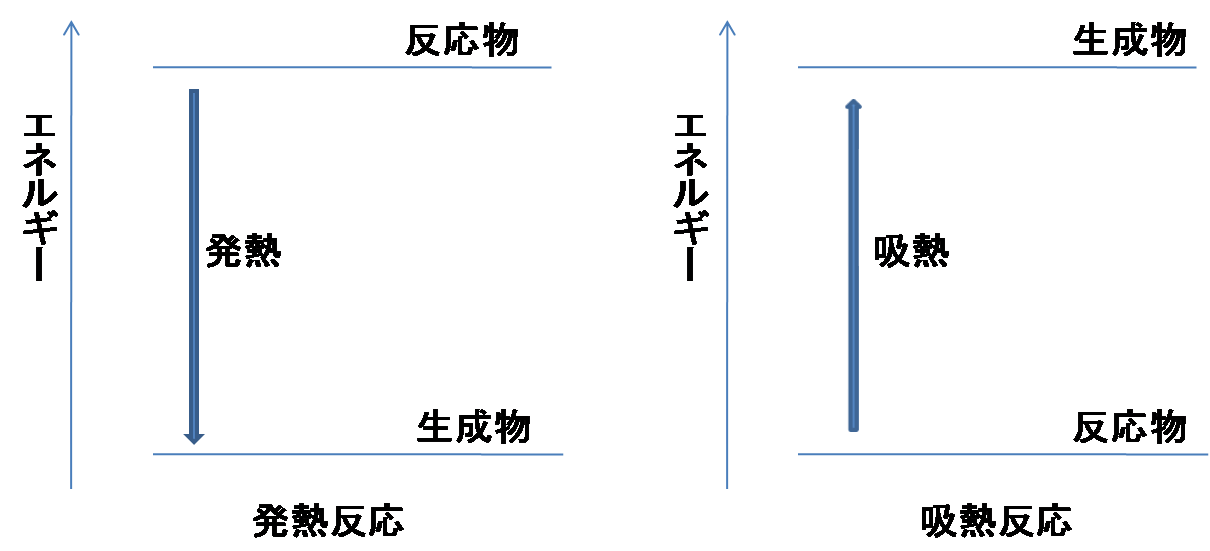


センター化学 お医者さんになろう



Wo 09 A1 Method For Producing 3 Mercaptoaniline Compound Lens



アセトアミノフェン Wikiwand


放課後化学講義室 今日の分子


芳香族化合物のモノニトロ化


窒素を含む芳香族化合物


放課後化学講義室 今日の分子


第79章 実験 ベンゼン



アセトアニリド 分子量 4
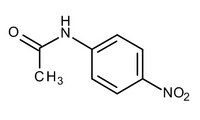


4 ニトロアセトアニリド Cas 104 04 1 00



Jpb2 ベンズイミダゾール化合物


薬剤師国家試験 薬学 薬学部 薬 くすり Be Pharmacist 基礎薬学


ニトロ化反応の条件とやり方 ネットdeカガク



メルカリ 基礎化学実験法18 参考書 600 中古や未使用のフリマ


有機反応機構 芳香族求電子置換反応



アニリンのニトロ化の生成過程 反応中間体の共鳴式 アニリンをニトロ 化学 教えて Goo


窒素を含む芳香族化合物
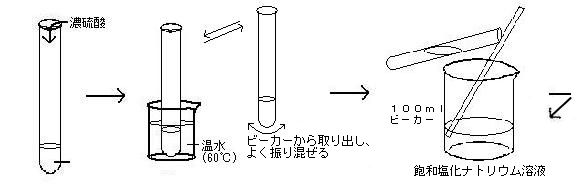


実験化学 52



アセトアミノフェン Wikiwand



ニトロ化スルホン化とは 触媒が濃硫酸である理由とは 化学受験テクニック塾


芳香族化合物のモノニトロ化



03 号 アセトアニリドベンツイミダゾロン系アゾ顔料およびその製造方法 Astamuse


お使いのブラウザーの検索機能を使って インタラクティブ有機化学英語 全体を検索して下さい A Ab Initio Calculations アブイニシオ計算 第一原理計算 Absolute Configuration 絶対配置 絶対立体配置 Absorbance 吸収度 吸光度 Absorption


ニトロ化反応の条件とやり方 ネットdeカガク


Ew 91回基礎完成


科学


P メトキシアセトアニリドを硝酸でニトロ化し4 メトキシ 2 ニトロ Yahoo 知恵袋



数学 化学講師 佐藤学による受験生に役立つ濃縮ポイントと Etc


アセトアニリドをニトロ化する際 固体のアセトアニリドに濃硫酸 Yahoo 知恵袋


窒素を含む芳香族化合物



吸光度測定で4 ニトロアニリンを用いて 質問失礼します 吸光度 化学 教えて Goo
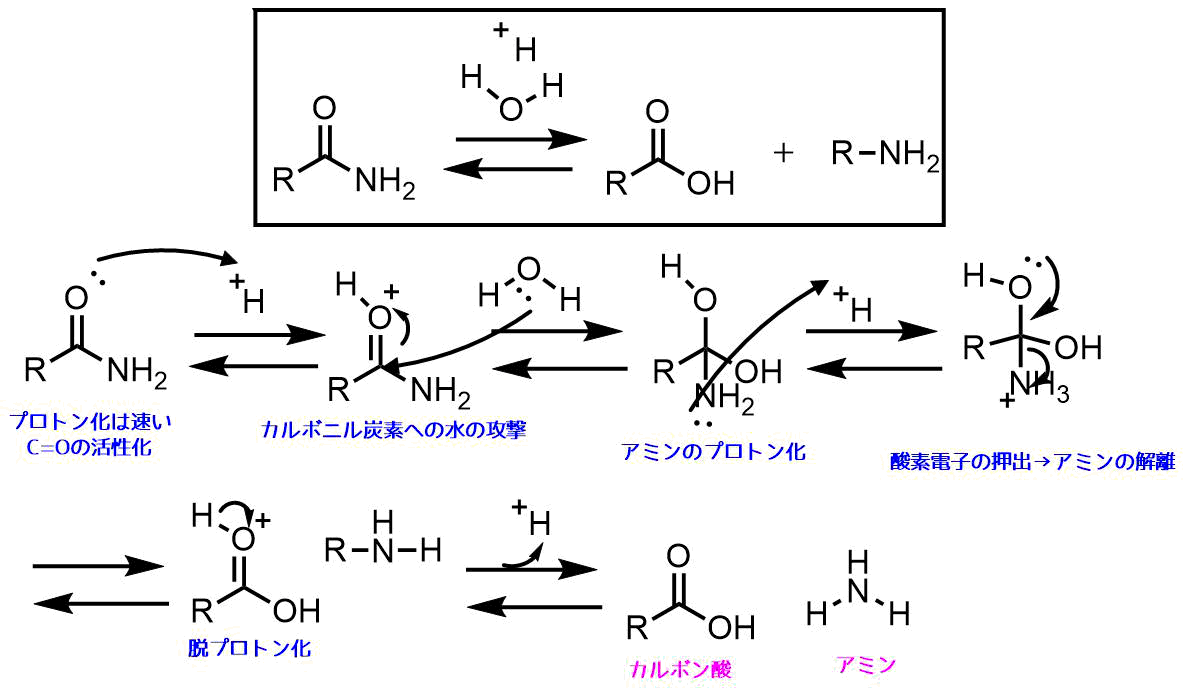


ニトロ化反応の条件とやり方 ネットdeカガク


放課後化学講義室 今日の分子


アセトアニリドをニトロ化する際 固体のアセトアニリドに濃硫酸 Yahoo 知恵袋



ニトロ化スルホン化とは 触媒が濃硫酸である理由とは 化学受験テクニック塾



化学質問集 その61 医薬品 化学 対症 療法 高校生 化学のノート Clear


ニトロアニリン 1
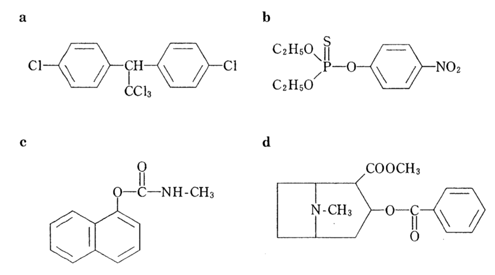


Kokushi Xslt Ver1 0


ここに フェノールのニトロ化はオルト パラ配向性であると書かれ Yahoo 知恵袋



0 件のコメント:
コメントを投稿